中科院药物所:九期一甘露特钠治疗阿尔茨海默病的药效原理分析!
老人防走失GPS定位器,防止阿尔茨海默病患者走失
老年人走丢了如何快速找回来?佩戴老人定位器,比其他任何手段都更有效果!
欢乐号200L老人专用GPS定位器,专为阿尔茨海默病老人和独居老人设计。除了精度高、体积小、重量轻、适合老人无感携带之外,它的续航能力远超同类产品,充一次电可以用1-2个月,不需要频繁充电,也避免了老人迷路了但是定位器没电了的困境。是子女防止老人走迷路的最合适的选择。

市面上很多老人GPS定位器,软件和硬件都是从车载GPS改过来的,别看宣传图上画只有纽扣大小,但实物有半个手机那么大,放在老人兜里很占空间。并且工作时间只有三五天,一旦忘记充电而老人走迷路了,就麻烦了。
老人手表,也能有效防止老人走失。老人手表的功能更加丰富,除了可以定位,还能打电话、看时间。老人手表好是好,但是耗电比较快,充一次电只能用一两天。如果老人忘记充电量就找不到他了。并且有些老人不习惯出门戴手表,不戴老人手表就丧失了老人防走失的功能了。
所以,专业老人GPS定位器要更靠谱一些。
★各大电商平台搜索“欢乐号”,报上我们的名号,领取更多优惠!
中科院药物所耿美玉揭示阿尔茨海默病潜在机制:肠道微生物群起神效。
“记忆的橡皮擦”,也许可以停下它残忍的“擦拭”了。国家药品监督管理局批准了甘露特钠胶囊(商品名:九期一,代号:GV-971)上市注册申请,用于轻度至中度阿尔茨海默病,改善患者认知功能。这款中国原创、国际首个靶向脑-肠轴的阿尔茨海默病治疗新药,也是全球首个糖类多靶抗阿尔茨海默症创新药物,通过优先审评审批程序在中国大陆的上市系全球首次上市。
“九期一”是由中国科学院上海药物研究所耿美玉研究员研发,将继续进行药理机制方面的研究和长期安全性有效性研究,完善寡糖的分析方法,按时提交有关试验数据。
阿尔茨海默病(AD),是一种慢性神经退行性疾病,通常随着时间的推移开始缓慢并逐渐恶化,这是60-70%的痴呆病例的原因。最常见的早期症状是难以记住最近发生的事件。随着疾病的进展,症状可能包括语言问题,情绪波动,失去动力,不管理自我护理和行为问题。越来越多的证据表明,淀粉样蛋白假说认为细胞外淀粉样蛋白β(Aβ)沉积是该疾病的根本原因。该病目前尚无有效药物。
2005年,孔令娜,耿美玉等人在中国的药学学报上发表了题为“酸性寡糖对阿尔茨海默病模型小鼠脑内基因表达的影响”的文章,酸性寡糖971改善AD模型小鼠学习记忆功能可能与DNA损伤修复、神经生长、突触可塑性、免疫应答等相关基因的表达变化有一定关系。
2017年,耿美玉等人在中国药理学与毒理学杂志报道了GV-971的2期临床结果:Ⅱ期临床研究表明,971 安全性好、能明显改善轻中度AD 患者认知功能障碍。最近,越来越多的证据表明肠道微生物的失调与阿尔茨海默病(AD)进展之间存在关联,但肠道微生物群在AD发病机制中的作用仍然模糊不清。
2019年9月6日,中国科学院上海药物所耿美玉团队在Cell Research 在线发表题为“Sodium oligomannate therapeutically remodels gut microbiota and suppresses gut bacterial amino acids-shaped neuroinflammation to inhibit Alzheimer’s disease progression”的研究论文,该研究使用AD小鼠模型,发现在AD进展期间,肠道微生物群组成的改变导致苯丙氨酸和异亮氨酸的外周积累,其刺激促炎性T辅助细胞1(Th1)细胞的分化和增殖。
脑浸润的外周Th1免疫细胞与M1小胶质细胞激活有关,导致AD相关的神经炎症。重要的是,在由AD引起的轻度认知障碍(MCI)的两个小的独立队列中也观察到苯丙氨酸和异亮氨酸浓度的升高以及血液中Th1细胞频率的增加。此外,GV-971,一种在中国的3期临床试验中表现出稳定和一致的认知改善的低聚甘油钠,抑制肠道失调和相关的苯丙氨酸/异亮氨酸积累,利用神经炎症并逆转认知障碍。总之,该研究结果突出了肠道微生物群失调促进神经炎症在AD进展中的作用,并提出了通过重塑肠道微生物群进行AD治疗的新策略。

尽管在治疗阿尔茨海默病(AD)方面做出了巨大努力,但过去几十年见证了β-淀粉样蛋白(Aβ) - 或以tau为中心的治疗策略在后期临床试验中的持续失败,这促使人们重新考虑新治疗策略。最近,大量研究表明肠道微生物群与宿主先天性和适应性免疫系统之间存在动态相互作用。肠道微生物群的生态失调可能危害宿主的免疫反应并促进其发展各种炎症性疾病。这似乎也是AD相关炎症的病例。
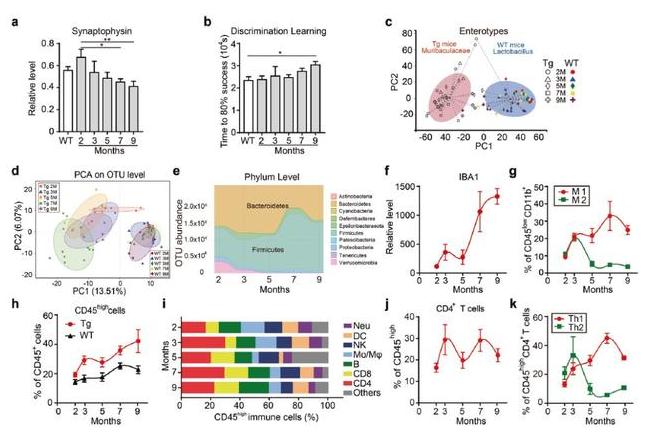
在5XFAD转基因(Tg)小鼠的疾病进展期间肠道生态失调和免疫细胞变化
来自动物和人类研究的新证据支持肠道微生物群的生态失调与AD发育过程中小胶质细胞激活之间的关联。例如,Minter等人发现肠道微生物多样性的失调影响神经炎症和淀粉样变性。此外,在AD患者的死后脑样本中发现肠道微生物群产生的脂多糖(LPS),外周注射LPS可促进小胶质细胞激活。所有证据表明,肠道微生物群可能参与调节AD中的小胶质细胞激活和神经炎症。除了小胶质细胞激活之外,在AD相关的神经炎症中浸润外周免疫细胞(例如CD4 +和CD8 + T细胞等)的作用也越来越受到重视。例如,据报道外周1型和17型T辅助细胞(Th1,Th17)与多种AD小鼠模型中炎性细胞因子的释放有关。

肠道微生物群是免疫细胞浸润和小胶质细胞激活所必需的
目前对AD进展中肠道和大脑之间联系的理解仍然非常有限。目前尚不清楚哪种类型的浸润免疫细胞在AD发育中具有功能参与。促进外周免疫细胞的潜在驱动力渗入大脑,导致住院神经炎症的增强,仍然模糊不清。此外,随着微生物群代谢物的重要性开始显现,必须理解在AD进展中将肠道微生物群与脑神经炎症联系起来的特定代谢物。

GV-971通过利用氨基酸代谢抑制神经炎症
本研究旨在探讨肠道微生物群与AD进展之间的机制联系,并探讨潜在的干预策略。为此,研究人员研究了肠道微生物群的动态变化与AD发展不同阶段的神经炎症之间的关联,并探讨了肠道微生物群与代谢物方面神经炎症之间可能的机制联系。特别地,研究人员利用称为GV-971的寡糖抗AD药物作为探针来评估,通过靶向肠道微生物群的潜在干预方法。GV-971是酸性线性寡糖的混合物,其范围从二聚体到十聚体(分子量高达~1kDa)。最近,GV-971在中国完成了AD的3期临床试验,并成功实现了其改善认知障碍的主要终点(未发表的数据)。
该研究使用AD小鼠模型,发现在AD进展期间,肠道微生物群组成的改变导致苯丙氨酸和异亮氨酸的外周积累,其刺激促炎性T辅助细胞1(Th1)细胞的分化和增殖。脑浸润的外周Th1免疫细胞与M1小胶质细胞激活有关,导致AD相关的神经炎症。重要的是,在由AD引起的轻度认知障碍(MCI)的两个小的独立队列中也观察到苯丙氨酸和异亮氨酸浓度的升高以及血液中Th1细胞频率的增加。

AD进展中肠 - 脑轴的示意图和干预策略
此外,GV-971,一种在中国的3期临床试验中表现出稳定和一致的认知改善的低聚甘油钠,抑制肠道失调和相关的苯丙氨酸/异亮氨酸积累,利用神经炎症并逆转认知障碍。总之,该研究结果突出了肠道微生物群失调促进神经炎症在AD进展中的作用,并提出了通过重塑肠道微生物群进行AD治疗的新策略。
新药效果如何?
临床试验表明可改善患者认知功能障碍。
自发现阿尔茨海默病100多年来,全球用于临床治疗的药物只有5款,临床获益不明显。
1998年~2017年间,全球有146个阿尔茨海默病症药物临床研发中心遭遇失败,40%夭折于早期临床阶段,39%在中期临床宣布失败,18%在后期临床失败。
世界范围内罗氏、礼来、大冢、默沙东及辉瑞强生等耳熟能详的大药企,都在阿尔茨海默病症的药物研发上寸步难进。其以接近100%的失败率,一直是最棘手的研发课题。
研发失败最重要原因之一是目前为止,人们对于阿尔茨海默病症发病的机制仍然搞不清楚。
目前主流的假设主要有β淀粉样蛋白假说和Tau蛋白假说两种,大部分抗轻中重度阿尔茨海默病症的药物和治疗方案都是围绕着这两个假设进行的。
“九期一”3期临床主要牵头研究者、上海交通大学医学院附属精神卫生中心肖世富教授指出,阿尔茨海默病目前的药物治疗还是对症治疗,且可供选用的药物不多,不能延缓或阻止病程进展。“九期一”的1、2、3期临床试验研究共有1199例受试者参加。其中3期临床试验由上海交通大学医学院附属精神卫生中心和北京协和医院牵头组织的全国34家三级甲等医院开展,共完成了818例受试者的服药观察。
在为期36周的多中心、随机双盲临床3期试验中,“九期一”能够明显改善轻、中度阿尔茨海默病患者的认知功能障碍。与安慰剂组相比,主要疗效指标认知功能改善显著。“九期一”对患者的认知功能具有起效快、呈持续稳健改善的特点,且安全性好,不良事件发生率与安慰剂组相当。
新药作用机制是什么?
通过重塑肠道菌群平衡改善认知功能障碍近年来,肠道微生物与疾病的研究成为生命科学领域的热门话题。中国科学技术大学教授朱书指出,目前,肠道菌群紊乱与一系列神经系统疾病包括自闭症、抑郁症、帕金森症、阿尔茨海默病等的关联性越来越清晰。因此,针对这些神经系统疾病,研究人员的目光已逐步从靶向中枢神经系统转移到靶向肠道微生物或者肠道免疫特征的研究上。
今年9月6日,“九期一”研究团队曾在学术期刊《细胞研究》(Cell Research)发表论文,披露研究过程。研究团队首先确认了在阿尔茨海默病进程中肠道菌群的改变与脑内侵润的免疫细胞具有相关性,并验证了“九期一”对阿尔茨海默病转基因小鼠认知功能障碍的改善作用。
研究发现,在阿尔茨海默病进程中,伴随Aβ的沉积以及Tau蛋白的磷酸化的发生,肠道菌群的组成发生变化,继而导致代谢产物异常,异常的代谢产物刺激外周免疫炎症,促使炎性免疫细胞Th1向大脑侵润,引起脑内M1型小胶质细胞的活化,导致阿尔茨海默病相关神经炎症的发生,最终导致认知功能障碍。
该药主要发明人、中国科学院上海药物研究所研究员耿美玉介绍,“九期一”通过重塑肠道菌群平衡,抑制肠道菌群特定代谢产物的异常增多,减少外周及中枢炎症,降低β淀粉样蛋白沉积和Tau蛋白过度磷酸化,从而改善认知功能障碍。
原文来自头条号:医学科普顾事